解答・解説を見る
■ 正解
3、4
■ 曲線矢印の基本ルール
- 電子は「電子を持っている側」から「電子不足の側」へ動く。
- 矢印の出発点:孤立電子対、結合電子(σ・π結合)。
- 矢印の終点:正電荷を帯びた原子、電子不足の原子、新たに結合ができる位置。
- +電荷(カルボカチオン)から矢印は出ない。
■ 各選択肢の解説
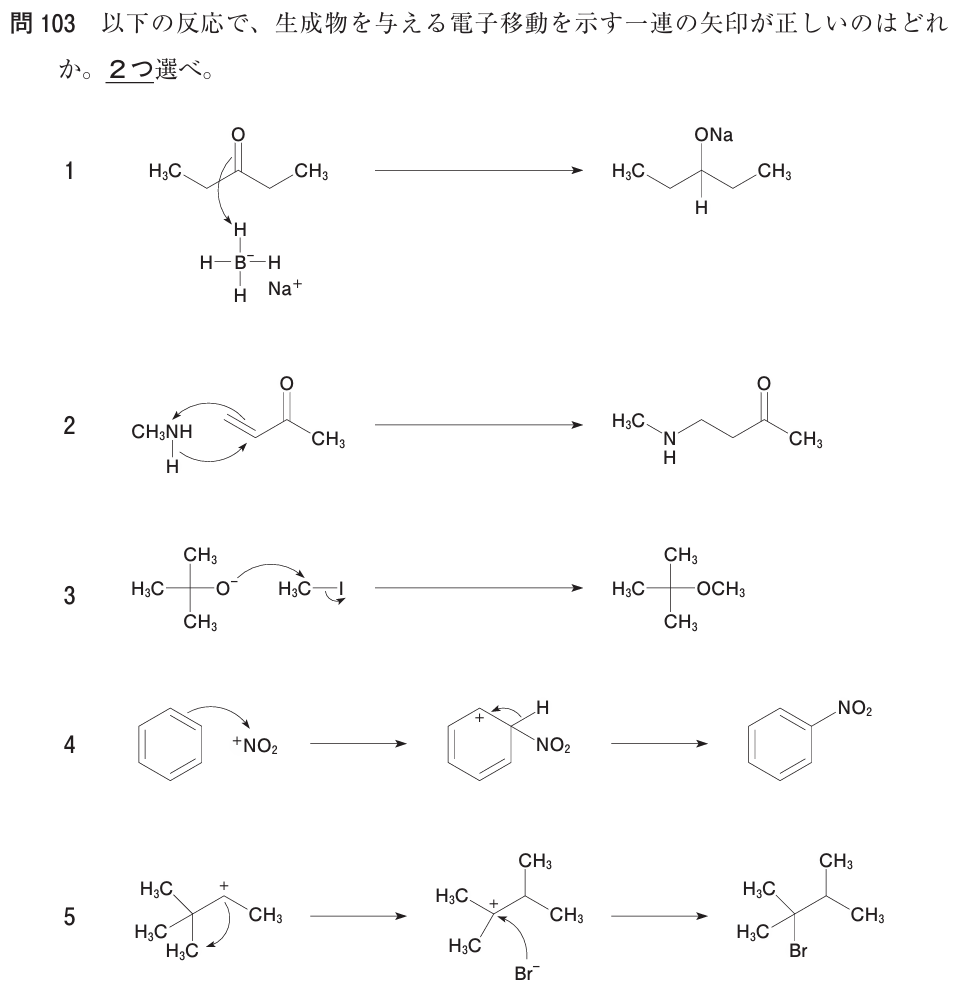
● 1:NaBH₄ によるカルボニルの還元(誤)
正しい機構では、B–H 結合の電子がカルボニル炭素へ移動し、C=O の π電子が酸素へ移動する。
しかし図では、電子の出発点・終点の取り方が不適切で、「電子を持つ結合 → 電子不足の炭素」という流れになっていない。
曲線矢印の文法として正しくないため誤り。
● 2:アミン + ケトン(イミン形成の初期段階)(誤)
本来の正しい機構は、N の孤立電子対 → C=O の炭素、C=O の π電子 → O という流れである。
しかし図では、C=C の結合から N に向かって矢印が描かれている。
C=C も電子リッチ、N も電子リッチであり、電子リッチ → 電子リッチという矢印は成立しない。
したがって、電子移動の向きが根本的に誤っており、不正解となる。
● 3:エーテル + CH₃I(SN2 反応)(正)
エーテル酸素の孤立電子対が CH₃I のメチル炭素を攻撃し、C–I 結合の電子が I に移動する典型的な SN2 機構である。
矢印は、O の孤立電子対 → メチル炭素、C–I 結合の電子 → I と描かれており、
「電子を持つ側 → 電子不足の側/結合が切れる側」というルールに完全に合致している。
よって正しい電子移動の矢印であり、正解。
● 4:ベンゼン + NO₂⁺(求電子芳香族置換)(正)
ベンゼン環の π電子が NO₂⁺ を攻撃し、σ錯体を経て脱プロトン化して芳香族性を回復する典型的な EAS 機構である。
矢印は、芳香環の π結合 → NO₂⁺、C–H 結合の電子 → 芳香環の π系 と描かれている。
いずれも「電子を持つ結合 → 電子不足の中心/π系への戻り」となっており、教科書通りの正しい機構である。
したがって正解。
● 5:カルボカチオンの転位 + Br⁻ の求核攻撃(誤)
この選択肢は、2級カルボカチオン → 3級カルボカチオンへの転位自体は概念として正しい(より安定なカチオンへの転位)。
しかし、図に描かれたアルキルシフトの曲線矢印の向きが逆になっている点が誤りである。
本来は、移動するアルキル基の C–C 結合の電子 → カルボカチオン中心(C⁺) と描くべきところ、
図ではC⁺ からアルキル基側へ矢印が向いており、「電子を持たない側から矢印が出ている」形になっている。
これは曲線矢印の文法に反するため、電子移動の表現として不正確であり、誤りとなる。
■ まとめ
- 曲線矢印は「電子を持つ側(孤立電子対・結合) → 電子不足の側」に向かう。
- 3:O の孤立電子対 → CH₃I の C(SN2)、4:π電子 → NO₂⁺(EAS)は文法的に正しい。
- 1・2・5 は、電子の出発点・終点、あるいは矢印の向きが曲線矢印のルールに反しているため誤り。


