【問題】
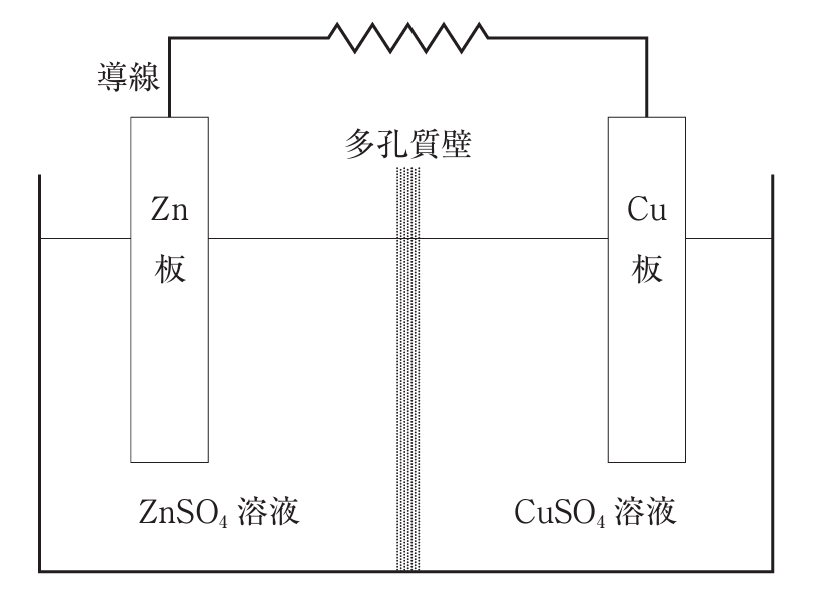
図はダニエル電池(Zn|ZnSO₄ ‖ CuSO₄|Cu)の模式図である。この電池の標準起電力として正しいのはどれか。
ただし、ZnとCuの半電池の標準電極電位はそれぞれ −0.763 V と +0.337 V とする。
- +0.213 V
- +0.426 V
- +1.100 V
- −0.426 V
- −1.100 V
解答・解説
【解答】
3 +1.100 V
【解説】
ダニエル電池は、亜鉛電極(Zn)を硫酸亜鉛溶液(ZnSO₄)に、銅電極(Cu)を硫酸銅溶液(CuSO₄)に浸し、両者を導線と多孔性隔壁で接続した構造をもつ電池である。
この電池では、亜鉛が電子を放出して亜鉛イオンとなる酸化反応が負極で進行し、銅イオンが電子を受け取って金属銅として析出する還元反応が正極で進行する。
負極(アノード)
Zn → Zn²⁺ + 2e⁻
正極(カソード)
Cu²⁺ + 2e⁻ → Cu
標準起電力 E° は、正極の標準電極電位から負極の標準電極電位を差し引くことで求められる。
E° = +0.337 V −(−0.763 V)
E° = +1.100 V
したがって、この電池の標準起電力は+1.100 Vである。


