解答・解説を見る
■ 正解
2
■ 解説
ベシル酸(besilic acid, besilate)は、医薬品の塩形成に用いられる酸であり、 その正体はベンゼンスルホン酸(benzene sulfonic acid)である。
医薬品では「○○ベシル酸塩(○○ besilate)」という形で登場し、 塩基性官能基(アミンなど)を中和して塩を形成するための強酸として利用される。
■ ベシル酸の特徴
- スルホン酸(–SO₃H)をもつ強酸
- カルボン酸(–CO₂H)よりはるかに酸性が強い
- アミン類と安定な塩を形成しやすい
- 医薬品の溶解性・安定性を改善する目的で用いられる
したがって、構造式として正しいのは ベンゼン環に –SO₃H が結合したもの(選択肢2)である。
■ 各選択肢の検討
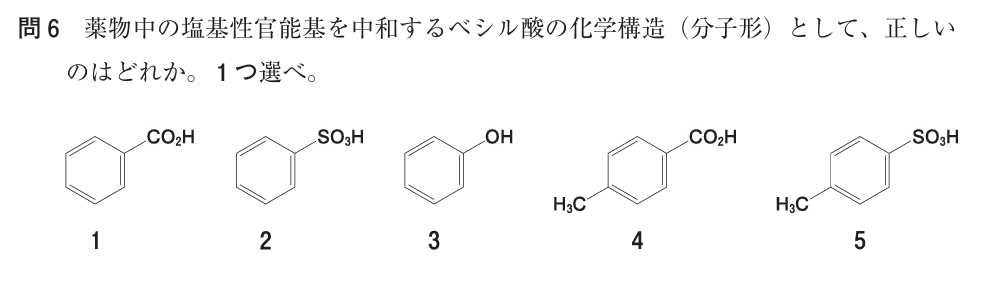
● 1:ベンゼンカルボン酸(安息香酸)(誤)
–CO₂H をもつが、これはカルボン酸であり酸性が弱い。 ベシル酸ではない。
● 2:ベンゼンスルホン酸(正)
–SO₃H をもつスルホン酸で、ベシル酸そのもの。 医薬品のベシル酸塩はこの構造の酸と塩基性薬物が結合したもの。
● 3:フェノール(–OH)(誤)
酸性はあるが非常に弱く、塩形成には不適。 ベシル酸とは全く異なる。
● 4:p-メチル安息香酸(誤)
カルボン酸であり、酸性が弱い。 ベシル酸ではない。
● 5:p-メチルベンゼンスルホン酸(誤)
スルホン酸で酸性は強いが、ベシル酸(ベンゼンスルホン酸)とは別物。 メチル基が付くと名称は「トルエンスルホン酸(トシル酸)」になる。
■ まとめ
- ベシル酸=ベンゼンスルホン酸(benzene sulfonic acid)。
- 構造は「ベンゼン環 − SO₃H」。
- 塩基性薬物と塩を作るために用いられる強酸。
- 正しい構造は選択肢2。


