解答・解説を見る
■ 正解
1
■ 解説
一酸化窒素(NO)は、生体内で血管拡張・神経伝達などに関わる重要な分子であり、 不対電子を1つ持つラジカル分子である。 この「奇数電子分子」である点が、ルイス構造式を判断する上で最も重要なポイントになる。
■ 電子数の確認
- N(窒素):5 個
- O(酸素):6 個
合計:11 個(奇数) → 奇数電子分子 → 必ず不対電子が存在する。
■ NO の結合の特徴
NO の実験的な結合次数は約 2.5とされ、 二重結合に近い結合性を持ちながら、不対電子が1つ残る構造が最も妥当である。
したがって、ルイス構造式としては N=O(二重結合)+ 不対電子(N側) という形が最も適切になる。
■ 各選択肢の検討
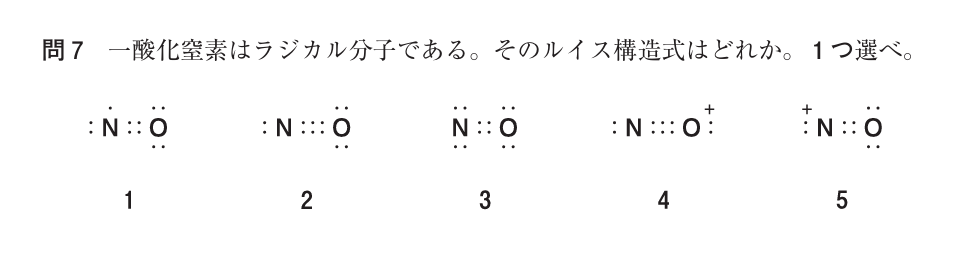
● 1:N=O に不対電子をもつ構造(正)
NO の電子数・結合次数・ラジカル性をすべて満たす。 最も妥当なルイス構造式。
● 2:三重結合(誤)
N≡O の三重結合では電子数が合わず、形式電荷も不自然。 NO の実際の結合次数(2.5)とも一致しない。
● 3:単結合(誤)
N–O の単結合では結合が弱すぎ、実際の結合距離・結合エネルギーと矛盾する。
● 4:O に正電荷がつく構造(誤)
酸素に正電荷がつくのは不自然で、NO の電子配置とも一致しない。
● 5:N に正電荷がつく構造(誤)
NO の電子数では成立しにくく、実際の分子特性とも合わない。
■ まとめ
- NO は奇数電子のラジカル分子。
- 結合次数は約 2.5 → 二重結合に近い。
- 最も妥当なルイス構造式は選択肢1。


