解答・解説を見る
■ 正解
1
■ 解説
アレニウスの式は、温度と反応速度定数 k の関係を示す基本式であり、薬物の分解反応、安定性評価、加速試験の解析に必ず用いられる。
温度依存性を理解することは、薬物の保存条件設定や有効期限の推定に直結する。
アレニウスの式:
k = A · exp(−Ea / (R T))
両辺の自然対数をとると、次の直線式になる。
ln k = −Ea/R · (1/T) + ln A
この式は、ln k(縦軸)と 1/T(横軸)をプロットすると直線になることを示している。 さらに、活性化エネルギー Ea は正の値であるため、傾き −Ea/R は必ず負になる。
■ 重要ポイント
- 直線になる → アレニウス式に従う反応
- 傾きは負 → 温度が上がるほど反応速度定数 k は増加する
- 1/T が増える(温度が下がる)と ln k は減少する → 右下がりの直線になる
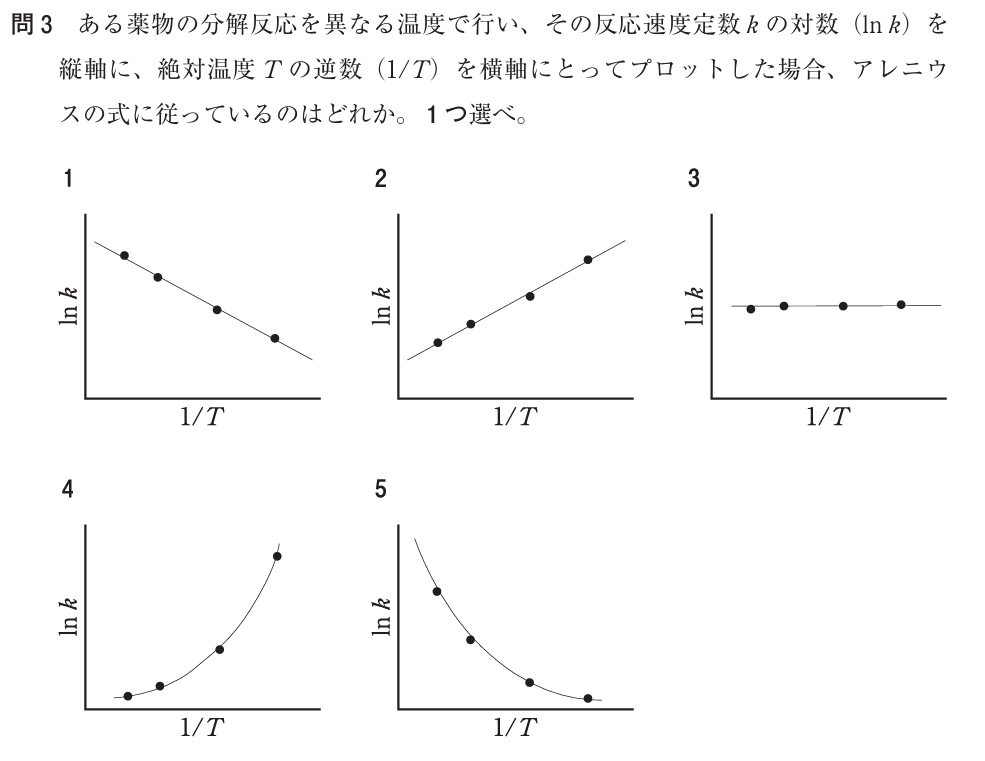
したがって、選択肢の中で「右下がりの直線」を示すグラフが正しい。
■ 各選択肢の検討
● 1:右下がりの直線(正)
アレニウス式の線形関係を正しく反映している。 活性化エネルギーが正である限り、この形になる。
● 2:右上がりの直線(誤)
傾きが正になるには Ea が負である必要があるが、通常の化学反応ではあり得ない。 温度上昇で反応が遅くなるという矛盾した挙動になる。
● 3:水平線(誤)
ln k が温度に依存しないことを意味する。 温度依存性が全くない反応は現実的ではない。
● 4:上に凸の曲線(誤)
複数の反応経路が競合する場合などに見られるが、アレニウス式の直線性とは一致しない。
● 5:下に凸の曲線(誤)
これも直線ではなく、アレニウス式の線形関係を満たさない。
■ まとめ
- ln k と 1/T のプロットは直線になる。
- 活性化エネルギーが正なので、傾きは必ず負。
- 正しいグラフは右下がりの直線(選択肢1)。


